Configuration du spectrophotomètre UV visible et loi de Beer-Lambert
Dans cet article, nous allons avoir une brève discussion sur la spectroscopie UV visible et la loi de Beer-Lambert.
Configuration du spectrophotomètre UV vis
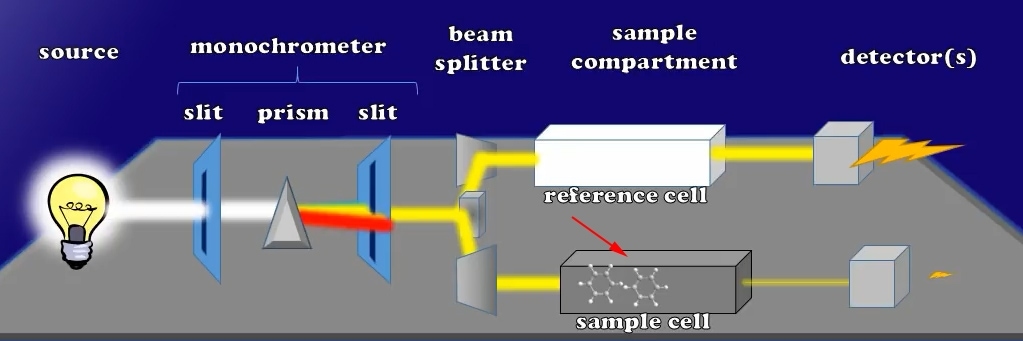
Pour commencer avec notre session ci-dessous est une conception technique qui est un type de configuration relativement typique pour un spectrophotomètre UV visible. Une variété de marques et de conceptions différentes sont disponibles pour fabriquer un spectrophotomètre, mais c’est l’une des méthodes les plus simples. Continuons à partir d’ici.

Configuration simple du spectrophotomètre UV vis
Pièces simples du spectrophotomètre
- Le premier composant est une lampe source qui peut être aussi basique qu’une lampe frontale de scooter ou une lampe au deutérium plus complexe ou même un style de lampe à arc au xénon.
- La partie suivante est un monochromateur, qui se compose de deux fentes séparées par un prisme ou une grille de diffraction. Nous parlerons de l’utilisation des fentes ci-dessous.
- Le dispositif suivant de ce spectrophotomètre est le soi-disant séparateur de faisceau qui divise le faisceau lumineux en deux faisceaux lumineux parallèles. Cette partie se compose de 2 prismes.
- Le composant suivant est le compartiment d’échantillon où se trouvent les cuves de référence et d’échantillon.
- Et le dernier élément est les détecteurs qui sont des capteurs qui peuvent être surveillés par un ordinateur pour transformer l’impact des photons en courant électrique.

5 parties de la conception du spectrophotomètre
Alors maintenant que nous avons identifié chacun des plus petits éléments à l’intérieur de notre spectrophotomètre simple. Allumons l’instrument et voyons ce qui va se passer.
Allumons la source de lumière de la lampe en créant différentes lumières dans une gamme de longueurs d’onde. Cette lumière passe à travers cette première fente monochromateur, ce qui garantit que tous les photons lumineux se déplaceront selon des voies parallèles; plus tard, lorsqu’ils atteindront le prisme, les lumières pourront se réfracter en un arc-en-ciel de couleur.
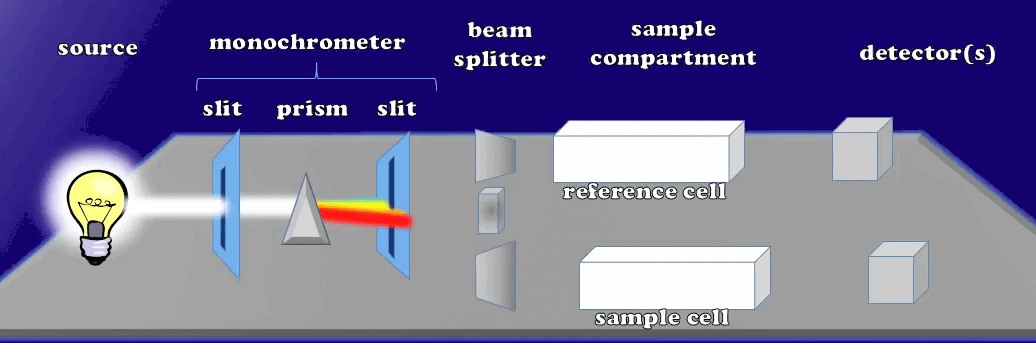
Les lumières parcourent des voies parallèles après le monochromateur
Ici, chaque longueur d’onde de la lumière se déplace vers l’autre fente, de sorte que seule une longueur d’onde de lumière prédéfinie est capable de passer à travers. Dans le monochromateur, la deuxième fente atteint le séparateur de faisceau qui transforme la lumière en deux faisceaux d’intensité égale. Ces deux faisceaux d’intensité égale traverseront le compartiment échantillon de différentes cuves: les cuves de référence et d’échantillon.
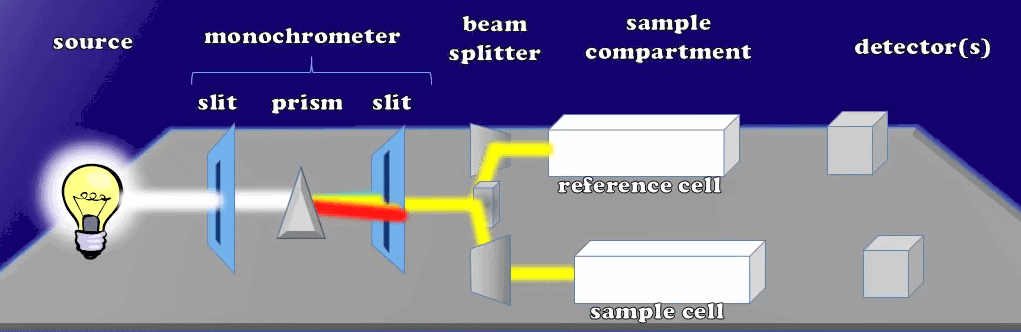
Les faisceaux traversent chaque cuvette avec une intensité égale
Alors que le faisceau sort de ces cuvettes et frappe le système de détection qui se déclenche pour créer un courant électrique, vous constaterez que les cuves de référence et d’échantillon ont la même intensité lumineuse à ce moment, par conséquent, le courant généré par chaque détecteur est le même.

Courant de sortie identique pour les deux cuvettes
Conséquences des données du spectrophotomètre
Ainsi, les deux intensités de courant détectées par chacun des deux détecteurs sont identiques dans ce cas. Si nous prenons en compte le rapport de l’intensité qui sort de la cuvette d’échantillon à celle qui sort de la cuvette de référence, nous pouvons voir que la transmission de notre cuvette d’échantillon est à 100% celle de la cuvette de référence. Nous allons donc cartographier ici cette transmission à 100% à concentration nulle.

je = Cuvette d’échantillon je 0 = Cuvette de référence
Ajoutons maintenant un petit échantillon à cette cuvette, qui pourrait absorber la lumière. Notez que l’intensité de la lumière de la cuvette d’échantillon diminue lorsque je fais cela. Il y a donc également une réduction du courant généré par son détecteur, respectivement.
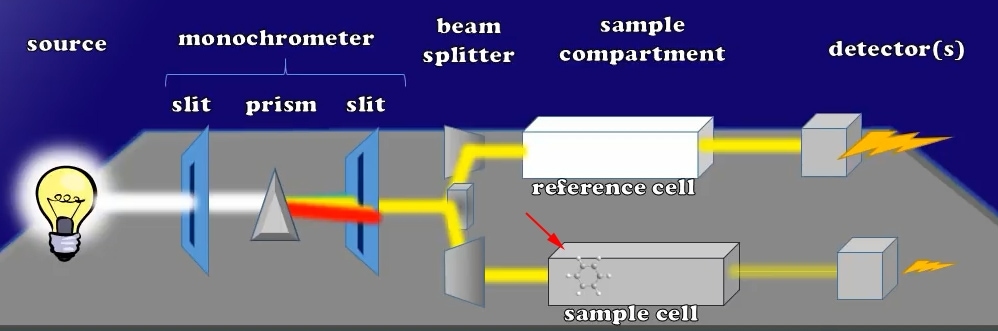
Diminution actuelle après l’ajout de l’échantillon
En tant que tel, le rapport d’intensité n’est plus de 100%, dans ce cas disons qu’il descend à 50% à une concentration X donnée.
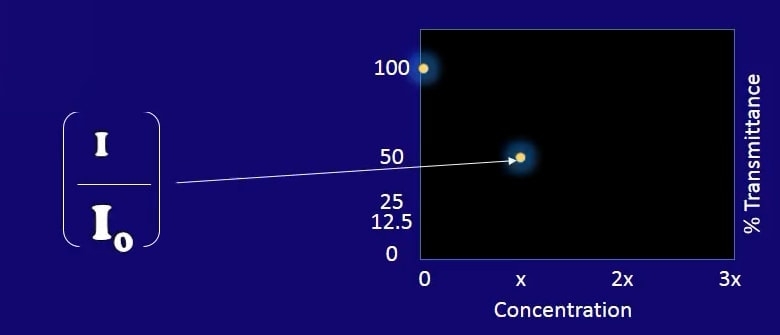
Le rapport d’intensité descend à 50%
Si j’ajoute un autre échantillon équivalent à la cuvette d’échantillon, cela réduit encore la force du courant. L’échantillon réduit de moitié l’intensité de la lumière traversant la cuve d’échantillon pour chaque concentration d’échantillon équivalente que nous ajoutons.
Deuxième échantillon ajouté
Calculons maintenant les nouvelles intensités de courant de l’échantillon et des cuvettes de référence, nous remarquerons qu’il s’agit d’une transmittance de 25% et d’une augmentation incrémentielle de la concentration en même temps.

je = Cuvette d’échantillon je 0 = Cuvette de référence
Ajouter l’échantillon une fois de plus, la cuvette d’échantillon entraîne une autre diminution de 50% et par conséquent un pourcentage de transmission de 12,5%. La concentration est maintenant de 3x.

je = Cuvette d’échantillon je 0 = Cuvette de référence
Nous avons maintenant suffisamment de données pour voir quelque chose de vraiment intéressant.
La relation entre le pourcentage de transmission et la concentration de l’échantillon n’est pas linéaire. C’est plutôt exponentiel.
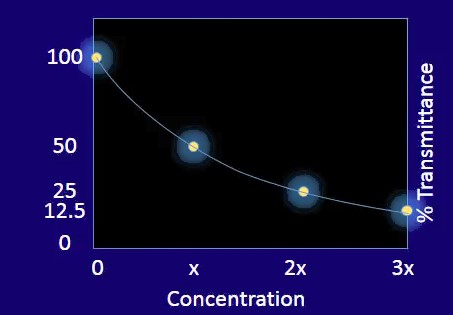
Bien que ces données soient très utiles, les chercheurs et les spectroscopistes préfèrent analyser les relations linéaires dans les résultats des données, aussi longtemps que possible, car cela rendra la discussion beaucoup plus claire et il est beaucoup plus facile de prévoir comment les choses se passeront si nous avons un tracé linéaire simple.
Bonjour Beer-Lambert Law
C’est là où Loi de Beer-Lambert devient utile. Vous pourriez avoir une idée que maintenant nous avons une connexion exponentielle entre le pourcentage de transmission et ma concentration.
Dans cette équation, nous pouvons voir que la concentration est un terme de l’exposant (conc).

August Beer a converti le pourcentage de transmission en une nouvelle unité appelée absorbance. En prenant le logarithme ou en réalité le logarithme négatif de la transmittance, nous avons l’équation suivante:

En utilisant le logarithme d’une fonction exponentielle, une fonction linéaire est créée. Les données sont donc considérablement plus faciles à regarder lorsqu’elles sont représentées sous forme d’absorbance plutôt que de transmittance. Sans oublier qu’en extrapolant ou en interpolant dans l’ensemble de données que nous avons collecté, il est beaucoup plus facile de prédire l’absorption exacte.

C’est pourquoi nous convertissons si souvent le pourcentage de transmittance en absorbance en effectuant une spectroscopie UV visible. C’est l’application de la loi de Beer-Lambert.
C’est tout pour le moment! Merci pour votre temps de lecture!
Présentateur: Professeur Davis de ChemSurvival
Lien vers la vidéo: https://www.youtube.com/watch?v=wxrAELeXlek
