Configurazione dello spettrofotometro UV visibile e legge di Beer-Lambert
In questo articolo avremo una breve discussione sulla spettroscopia UV visibile e la legge di Beer-Lambert.
Configurazione dello spettrofotometro UV vis
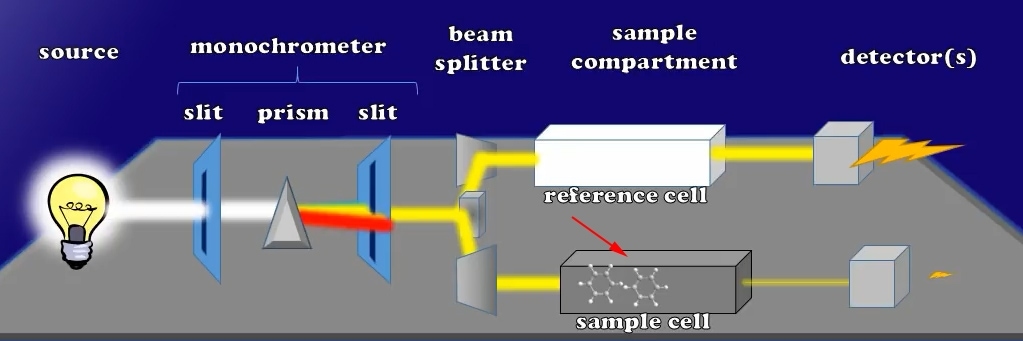
Per iniziare con la nostra sessione di seguito è un progetto ingegneristico che è un tipo di configurazione relativamente tipico per uno spettrofotometro UV visibile. È disponibile una varietà di marchi e design diversi per produrre uno spettrofotometro, ma questo è uno dei modi più semplici. Continuiamo da qui.

Configurazione semplice dello spettrofotometro UV vis
Parti semplici dello spettrofotometro
- Il primo componente è una lampada sorgente che può essere semplice come un faro di uno scooter o una lampada al deuterio più complessa o persino una lampada ad arco allo xeno.
- La parte successiva è un monocromatore, che consiste in due fenditure separate da un prisma o da una griglia di diffrazione. Di seguito parleremo dell’uso delle fessure.
- Il dispositivo successivo di questo spettrofotometro è il cosiddetto beam splitter che divide il fascio di luce in due fasci di luce paralleli. Questa parte è composta da 2 prismi.
- Il componente successivo è lo scomparto del campione in cui si trovano le cuvette di riferimento e del campione.
- E l’elemento finale sono i rivelatori che sono sensori che possono essere monitorati da un computer per trasformare l’impatto dei fotoni in corrente elettrica.

5 parti del design dello spettrofotometro
Quindi ora che abbiamo identificato ciascuno degli elementi più piccoli all’interno del nostro semplice spettrofotometro. Accendiamo lo strumento e vediamo cosa succederà.
Accendiamo la sorgente luminosa della lampada creando luci diverse in una gamma di lunghezze d’onda. Questa luce passa attraverso questa prima fenditura monocromatrice, che assicura che tutti i fotoni luminosi viaggeranno lungo percorsi paralleli; in seguito, quando raggiungeranno il prisma, le luci potranno rifrangersi in un arcobaleno di colori.
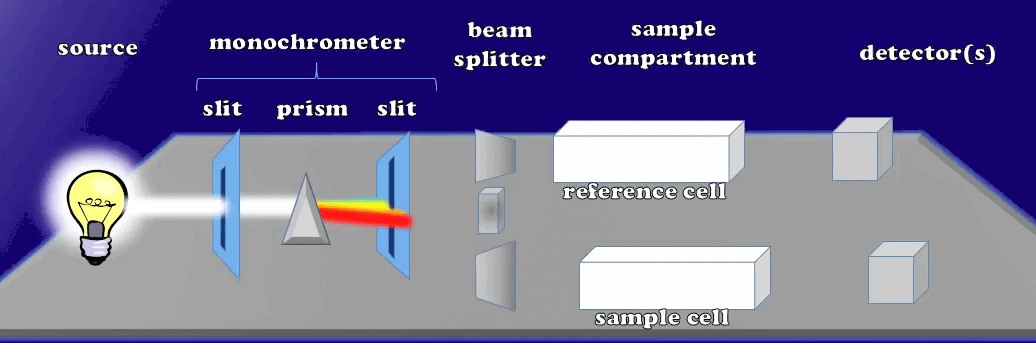
Le luci viaggiano su percorsi paralleli dopo il monocromatore
Qui ogni lunghezza d’onda della luce si sposta sull’altra fenditura, in modo che solo una lunghezza d’onda della luce preimpostata è in grado di passare attraverso. Nel monocromatore la seconda fenditura raggiunge il divisore di fascio che trasforma la luce in due fasci di uguale intensità. Questi due fasci di uguale intensità passeranno attraverso il compartimento del campione di diverse cuvette: la cuvetta di riferimento e quella del campione.
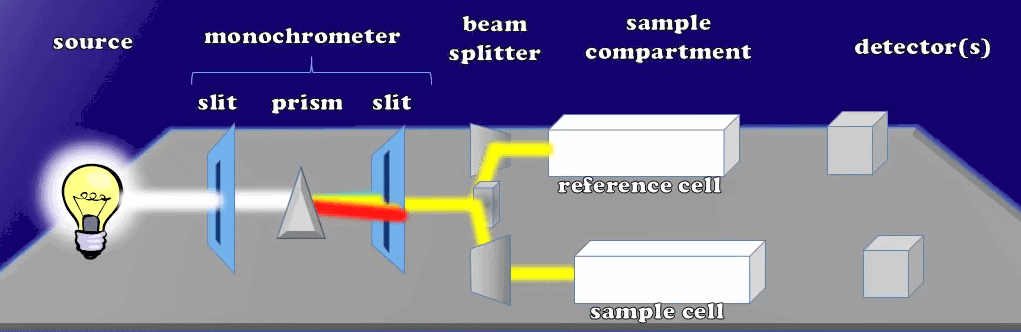
I raggi attraversano ogni cuvetta con la stessa intensità
Mentre il raggio esce da queste cuvette e colpisce il sistema di rilevamento che spara per creare una corrente elettrica, scoprirai che entrambe le cuvette di riferimento e campione hanno la stessa intensità di luce in questo momento, di conseguenza la corrente generata da ciascun rivelatore è la stesso.

Corrente di uscita identica per entrambe le cuvette
Conseguenze dei dati dello spettrofotometro
Quindi sia l’intensità di corrente rilevata da ciascuno dei due rilevatori è identica in questo caso. Se prendiamo in considerazione il rapporto tra l’intensità che esce dalla cuvetta d’analisi e quella che lascia la cuvetta di riferimento, possiamo vedere che la trasmissione della nostra cuvetta d’analisi è del 100% quella della cuvetta di riferimento. Pertanto, mapperemo questa trasmissione al 100% qui a concentrazione zero.

io = Cuvetta campione io 0 = Cuvetta di riferimento
Aggiungiamo ora un piccolo campione a quella cuvetta, che potrebbe assorbire la luce. Notare che l’intensità della luce dalla cuvetta del campione diminuisce quando si esegue questa operazione. Si ha quindi anche una riduzione della corrente generata rispettivamente dal suo rivelatore.
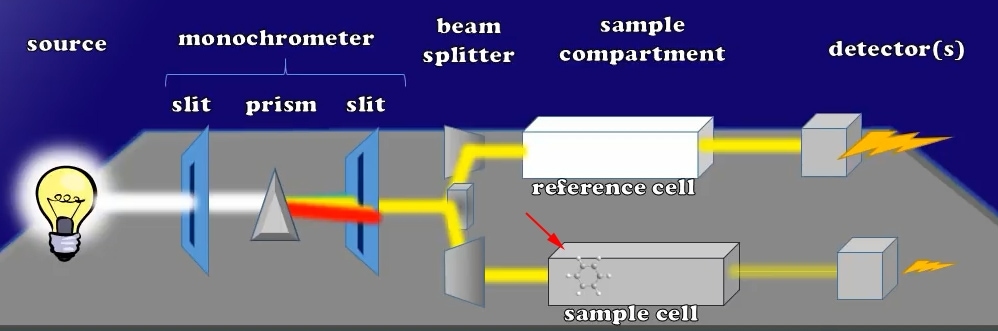
Diminuzione corrente dopo l’aggiunta del campione
In quanto tale, il rapporto di intensità non è più del 100%, in questo caso diciamo che scende al 50% a una data concentrazione X.
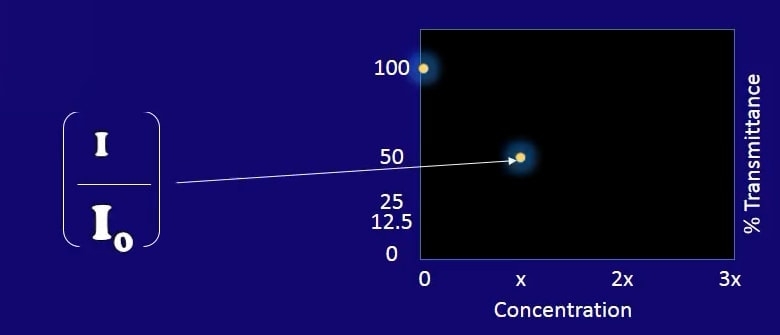
Il rapporto di intensità scende al 50%
Se aggiungo un altro campione equivalente alla cuvetta del campione che riduce ulteriormente la forza attuale. Il campione riduce l’intensità della luce che passa attraverso la cuvetta del campione solo della metà per ogni concentrazione di campione equivalente che aggiungiamo.
Secondo campione aggiunto
Ora calcoliamo le nuove intensità di corrente del campione e delle cuvette di riferimento, noteremo che è il 25% di trasmittanza e un aumento incrementale della concentrazione allo stesso tempo.

io = Cuvetta campione io 0 = Cuvetta di riferimento
Aggiungere il campione ancora una volta la cuvetta del campione porta ad un’altra diminuzione del 50% e di conseguenza a una trasmissione percentuale del 12,5%. La concentrazione è ora 3x.

io = Cuvetta campione io 0 = Cuvetta di riferimento
Ora abbiamo dati sufficienti per vedere qualcosa di veramente interessante.
La relazione tra la percentuale di trasmissione e la concentrazione del campione non è lineare. È invece esponenziale.
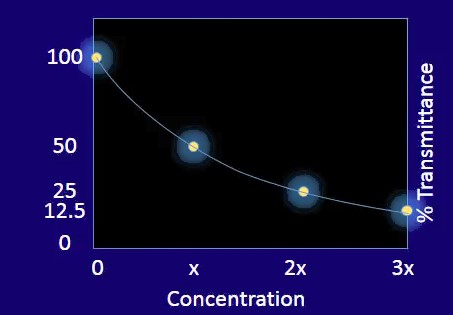
Sebbene questi dati siano molto utili, i ricercatori e gli spettroscopisti preferiscono analizzare le relazioni lineari all’interno dei risultati dei dati, finché è possibile, perché questo renderà la discussione molto più chiara ed è molto più facile prevedere come andranno le cose se avremo un trama lineare semplice.
Ciao Beer-Lambert Law
Ecco dove Legge di Beer-Lambert diventa utile. Potresti avere un’idea che ora abbiamo una connessione esponenziale tra la percentuale di trasmissione e la mia concentrazione.
In questa equazione, possiamo vedere che la concentrazione è un termine nell’esponente (conc).

August Beer ha convertito la percentuale di trasmittanza in una nuova unità chiamata assorbanza. Prendendo il logaritmo o in realtà il logaritmo negativo della trasmittanza abbiamo la seguente equazione:

Utilizzando il logaritmo di una funzione esponenziale viene creata una funzione lineare. I dati sono quindi notevolmente più facili da esaminare quando tracciati come assorbanza piuttosto che come trasmittanza. Per non parlare del fatto che estrapolando o interpolando all’interno del set di dati che abbiamo raccolto, è molto più facile prevedere l’esatto assorbimento.

Questo è il motivo per cui convertiamo così spesso la trasmittanza percentuale in assorbanza eseguendo la spettroscopia UV visibile. Questa è l’applicazione della legge di Beer-Lambert.
È tutto per ora! Grazie per il tuo tempo a leggere!
Presentatore: Professor Davis di ChemSurvival
Link al video: https://www.youtube.com/watch?v=wxrAELeXlek
